Artikel ini sudah memiliki daftar referensi, bacaan terkait, atau pranala luar, tetapi sumbernya belum jelas karena belum menyertakan kutipan pada kalimat. |
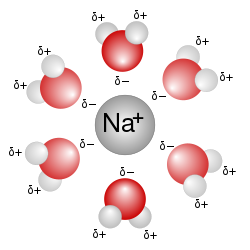
Larutan berair adalah larutan yang pelarutnya adalah air. Larutan ini sering kali diberi tanda (aq) dalam persamaan kimia. Contohnya, larutan garam meja atau natrium klorida dapat ditulis NaCl (aq). Kata "berair" di sini berarti terkait dengan, mirip dengan, atau larut dalam air. Air adalah pelarut yang sangat baik dan juga berlimpah di alam, sehingga air sering digunakan sebagai pelarut dalam bidang kimia.
Bahan hidrofobik tidak terlarut dalam air, sementara bahan hidrofilik dapat larut. Contoh bahan hidrofilik ialah natrium klorida. Asam dan basa adalah larutan berair seperti yang tertera dalam definisi Arrheniusnya.
Keterlarutan suatu bahan di dalam air dapat diketahui dari kemampuan bahan tersebut untuk menyamai atau melebihi kekuatan daya tarikan yang dihasilkan oleh molekul air di antara satu sama lain. Jika bahan tersebut tidak mempunyai kemampuan untuk larut dalam air, bahan terbut akan membentuk endapan.
Larutan berair yang dapat menghantarkan arus listrik dengan efektif mengandung elektrolit yang kuat, manakala yang tidak dapat menghantarkan listrik dengan baik dianggap mempunyai elektrolit yang lemah. Elektrolit yang kuat adalah bahan yang sepenuhnya terionisasi di dalam air/
Bahan non-elektrolit adalah bahan yang dapat larut dalam air tetapi tetap mempertahankan integritas molekulnya (tidak terpisah menjadi ion-ion). Contohnya adalah gula, urea, gliserol, dan metilsulfonilmetana (MSM).
Rujukan
sunting- Zumdahl S. 1997. Chemistry. 4th ed. Boston: Houghton Mifflin Company. p 133-145.








