| |||

| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Piperidina
| |||
| Nama IUPAC (preferensi)
Piperidina[2] | |||
| Nama lain
Heksahidropiridina
Azasikloheksana Pentametilenaamina Azinana | |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
| KEGG | |||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| UNII | |||
| Nomor UN | 2401 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C5H11N | |||
| Massa molar | 85,15 g·mol−1 | ||
| Penampilan | Cairan tak berwarna | ||
| Bau | Seperti air mani,[3] berbau amis seperti amonia, tajam | ||
| Densitas | 0,862 g/mL | ||
| Titik lebur | −7 °C (19 °F; 266 K) | ||
| Titik didih | 106 °C (223 °F; 379 K) | ||
| Dapat bercampur | |||
| Keasaman (pKa) | 11,22 (terprotonasi)[4] | ||
| −64,2·10−6 cm3/mol | |||
| Viskositas | 1,573 cP pada 25 °C | ||
| Bahaya | |||
| Lembar data keselamatan | MSDS1 | ||
| Piktogram GHS |   
| ||
| Keterangan bahaya GHS | {{{value}}} | ||
| H225, H311, H314, H331 | |||
| P210, P233, P240, P241, P242, P243, P260, P261, P264, P271, P280, P301+P330+P331, P302+P352, P303+P361+P353, P304+P340, P305+P351+P338, P310, P311, P312, P321, P322, P361, P363, P370+P378, P403+P233, P403+P235, P405, P501 | |||
| Legal status | |||
| Senyawa terkait | |||
Senyawa terkait
|
Piridina Pirolidina Piperazina Fosforinana Arsinana | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Piperidina adalah senyawa organik dengan rumus molekul (CH2)5NH. Amina heterosiklik ini terdiri dari cincin beranggota enam yang mengandung lima jembatan metilena (–CH2–) dan satu jembatan amina (–CH2–). Ini merupakan cairan tidak berwarna dengan bau yang tidak sedap seperti sperma manusia, khas amina.[5] Namanya berasal dari nama genus Piper, yang merupakan kata Latin untuk "lada".[6] Meskipun piperidina adalah senyawa organik umum, ia paling dikenal sebagai elemen struktur representatif dalam banyak obat-obatan dan alkaloid, seperti solenopsin yang terbentuk secara alami.[7]
Produksi
suntingPiperidina pertama kali dilaporkan pada tahun 1850 oleh ahli kimia Skotlandia Thomas Anderson, dan secara independen pada tahun 1852 oleh ahli kimia Prancis Auguste Cahours selaku yang menamainya.[8][9][10] Keduanya memperoleh piperidina dengan mereaksikan piperin dengan asam nitrat.
Secara industri, piperidina diproduksi melalui hidrogenasi piridina, biasanya menggunakan katalis molibdenum disulfida:[11]
- C5H5N + 3 H2 → C5H10NH
Piridina juga dapat direduksi menjadi piperidina melalui reduksi Birch yang dimodifikasi menggunakan natrium dalam etanol.[12]
Keberadaan piperidina dan turunannya secara alami
suntingPiperidina sendiri telah diperoleh dari lada,[13][14] dari Psilocaulon absimile (keluarga Aizoaceae),[15] dan Petrosimonia monandra.[16]
Motif struktur piperidina terdapat dalam banyak alkaloid alami, termasuk piperin yang memberikan rasa pedas pada lada. Hal ini memberi nama pada senyawa piperidina. Contoh lain adalah toksin semut api yakni solenopsin,[17] analog nikotin anabasin dari tembakau pohon (Nicotiana glauca), lobelina dari Lobelia inflata, dan alkaloid beracun koniina dari hemlock beracun, yang digunakan untuk membunuh Socrates.[18]
Konformasi
suntingPiperidina lebih menyukai konformasi kursi, mirip dengan sikloheksana. Tidak seperti sikloheksana, piperidina memiliki dua konformasi kursi yang dapat dibedakan: satu dengan ikatan N–H pada posisi aksial, dan yang lainnya pada posisi ekuatorial. Setelah banyak kontroversi selama tahun 1950-an–1970-an, konformasi ekuatorial ditemukan lebih stabil sebesar 0,72 kkal/mol dalam fase gas.[19] Dalam pelarut nonpolar, kisaran antara 0,2 dan 0,6 kkal/mol telah diperkirakan, tetapi dalam pelarut polar konformer aksial mungkin lebih stabil.[20] Kedua konformer tersebut saling berubah dengan cepat melalui inversi nitrogen; Energi bebas pengaktifan untuk proses ini diperkirakan sebesar 6,1 kkal/mol, jauh lebih rendah daripada 10,4 kkal/mol untuk inversi cincin.[21] Dalam kasus N-metilpiperidina, konformasi ekuatorial lebih disukai sebesar 3,16 kkal/mol,[19] yang jauh lebih besar daripada preferensi pada metilsikloheksana, yakni sebesar 1,74 kkal/mol.
 |

|
| Konformasi aksial | Konformasi ekuatorial |
Reaksi
suntingPiperidina banyak digunakan untuk mengubah keton menjadi enamina.[22] Enamina yang berasal dari piperidina merupakan substrat dalam reaksi alkilasi enamina Stork.[23]
Setelah perlakuan dengan kalsium hipoklorit, piperidina berubah menjadi N-kloropiperidina, kloramina dengan rumus C5H10NCl. Kloramina yang dihasilkan mengalami dehidrohalogenasi untuk menghasilkan imina siklik.[24]
Kegunaan
suntingPiperidina digunakan sebagai pelarut dan sebagai basa. Hal yang sama berlaku untuk turunan tertentu: N-formilpiperidina adalah pelarut aprotik polar dengan kelarutan hidrokarbon yang lebih baik daripada pelarut amida lainnya; dan 2,2,6,6-tetrametilpiperidina adalah basa yang sangat terhalang secara sterik, berguna karena nukleofilisitasnya yang rendah dan kelarutan yang tinggi dalam pelarut organik.
Penggunaan industri yang signifikan dari piperidina adalah untuk produksi dipiperidinil ditiuram tetrasulfida, yang digunakan sebagai akselerator vulkanisasi belerang karet alami.[11]
Daftar obat piperidina
sunting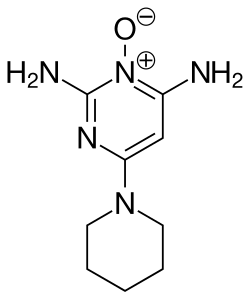
Piperidina dan turunannya merupakan bahan baku yang umum dalam farmasi[25] dan bahan kimia halus. Struktur piperidina ditemukan dalam, misalnya:
- Pikaridin (Pengusir serangga)
- SSRI (penghambat penyerapan kembali serotonin selektif)
- Stimulan dan nootropika:
- Antagonis/agonis invers reseptor histamin 1 (H1):
- Antagonis/agonis invers reseptor histamin 3 (H3):
- SERM (modulator reseptor estrogen selektif)
- Vasodilator
- Antipsikotik:
- Opioid:
- Dipipanona
- Fentanil dan analognya
- Loperamida
- Petidina (meperidina)
- Prodina
- Arilsikloheksilamina:
- Fensiklidina dan analognya
- Senjata kimia antikolinergik
- Ditran
- N-Metil-3-piperidil benzilat (JB-336, BZ)
Piperidina juga umum digunakan dalam reaksi degradasi kimia seperti pengurutan DNA dalam pemecahan nukleotida termodifikasi tertentu. Piperidina juga umum digunakan sebagai basa untuk deproteksi asam amino Fmoc yang digunakan dalam sintesis peptida fase padat.
Piperidina terdaftar sebagai prekursor Tabel II di bawah Konvensi Perserikatan Bangsa-Bangsa tentang Pemberantasan Perdagangan Narkotika dan Zat Psikotropika Ilegal karena penggunaannya (puncaknya pada tahun 1970-an) dalam pembuatan fensiklidina secara ilegal.[26]
Referensi
sunting- ^ "International Chemical Safety Card 0317". 28 January 2024.
- ^ "Front Matter". Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. hlm. 142. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ Amoore, J. E. (1975). "Specific anosmia to 1-pyrroline: The spermous primary odor". J. Chem. Ecol. 1 (3): 299–310. Bibcode:1975JCEco...1..299A. doi:10.1007/BF00988831. S2CID 19318345.
- ^ Hall, H. K. (1957). "Correlation of the Base Strengths of Amines". J. Am. Chem. Soc. 79 (20): 5441–5444. Bibcode:1957JAChS..79.5441H. doi:10.1021/ja01577a030.
- ^ Frank Johnson Welcher (1947). Organic Analytical Reagents. D. Van Nostrand. hlm. 149.
- ^ Senning, Alexander (2006). Elsevier's Dictionary of Chemoetymology. Amsterdam: Elsevier. ISBN 978-0-444-52239-9.
- ^ Pianaro, Adriana; Fox, Eduardo G.P.; Bueno, Odair C.; Marsaioli, Anita J. (May 2012). "Rapid configuration analysis of the solenopsins". Tetrahedron: Asymmetry (dalam bahasa Inggris). 23 (9): 635–642. doi:10.1016/j.tetasy.2012.05.005.
- ^ Warnhoff, Edgar W. (1998). "When piperidine was a structural problem" (PDF). Bulletin for the History of Chemistry. 22 (22): 29–34. doi:10.70359/bhc1998n22p029.

- ^ Anderson, Thomas (1850). "Vorläufiger Bericht über die Wirkung der Salpetersäure auf organische Alkalien" [Preliminary report on the effect of nitric acid on organic alkalis]. Annalen der Chemie und Pharmacie. 75: 80–83. doi:10.1002/jlac.18500750110.

- ^ Cahours, Auguste (1852). "Recherches sur un nouvel alcali dérivé de la pipérine" [Investigations of a new alkali derived from piperine]. Comptes Rendus. 34: 481–484.
L'alcali nouveau dérivé de la pipérine, que je désignerai sous le nom de 'pipéridine',… (The new alkali derived from piperine, which I will designate by the name of 'piperidine',…

- ^ a b Eller, Karsten; Henkes, Erhard; Rossbacher, Roland; Höke, Hartmut (2005), "Amines, Aliphatic", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a02_001
- ^ Marvel, C. S.; Lazier, W. A. (1929). "Benzoyl Piperidine". Org. Synth. 9: 16. doi:10.15227/orgsyn.009.0016.
- ^ Späth; Englaender (1935). "Über das Vorkommen von Piperidin im schwarzen Pfeffer". Chemische Berichte. 68 (12): 2218–2221. doi:10.1002/cber.19350681211.
- ^ Pictet, Amé; Pictet, René (1927). "Sur l'alcaloïde volatil du poivre". Helvetica Chimica Acta. 10: 593–595. Bibcode:1927HChAc..10..593P. doi:10.1002/hlca.19270100175.
- ^ Rimington, Claude (1934). "Psilocaulon absimile N.E.Br. as a stock poison". South African Journal of Science. 31: 184–193. hdl:10520/AJA00382353_6425.
- ^ Juraschewski; Stepanov (1939). J. Gen. Chem. USSR. 9: 1687.
- ^ Arbiser, J. L.; Kau, T.; Konar, M.; et al. (2007). "Solenopsin, the alkaloidal component of the fire ant (Solenopsis invicta), is a naturally occurring inhibitor of phosphatidylinositol-3-kinase signaling and angiogenesis". Blood. 109 (2): 560–5. doi:10.1182/blood-2006-06-029934. PMC 1785094. PMID 16990598.
- ^ Thomas Anderson Henry (1949). The Plant Alkaloids (Edisi 4th). The Blakiston Company.
- ^ a b Carballeira, Luis; Pérez Juste, Ignacio (1998). "Influence of calculation level and effect of methylation on axial/equatorial equilibria in piperidines". Journal of Computational Chemistry. 19 (8): 961–976. doi:10.1002/(SICI)1096-987X(199806)19:8<961::AID-JCC14>3.0.CO;2-A. S2CID 98028598.
- ^ Blackburne, Ian D.; Katritzky, Alan R.; Yoshito Takeuchi (1975). "Conformation of piperidine and of derivatives with additional ring hetero atoms". Acc. Chem. Res. 8 (9): 300–306. doi:10.1021/ar50093a003.
- ^ Anet, F. A. L.; Yavari, Issa (1977). "Nitrogen inversion in piperidine". J. Am. Chem. Soc. 99 (8): 2794–2796. Bibcode:1977JAChS..99.2794A. doi:10.1021/ja00450a064.
- ^ (1990) "Spiro[5.7trideca-1,4-dien-3-one]". Org. Synth.; Coll. Vol. 7: 473.
- ^ Smith, Michael B.; March, Jerry (2001). March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (Edisi 5th). Wiley-Interscience. ISBN 978-0-471-58589-3.
- ^ (1977) "2,3,4,5-Tetrahydropyridine Trimer". Org. Synth. 56: 118.
- ^ Vitaku, E.; D. T. Smith; J. T. Njardarson (2014). "Analysis of the Structural Diversity, Substitution Patterns, and Frequency of Nitrogen Heterocycles among U.S. FDA Approved Pharmaceuticals". Journal of Medicinal Chemistry. 57 (24): 10257–10274. doi:10.1021/jm501100b. PMID 25255204.
- ^ "List of Precursors and Chemicals Frequently Used in the Illicit Manufacture of Narcotic Drugs and Psychotropic Substances Under International Control" (PDF). International Narcotics Control Board. Diarsipkan dari asli (PDF) tanggal 2008-02-27.
Pranala luar
sunting Media terkait Piperidine di Wikimedia Commons
Media terkait Piperidine di Wikimedia Commons










